|
Libero51
| Inviato il: 19/3/2009,15:07
|
Ciao a tutti, non penso di essere veramente all'altezza di affrontare un tema cosě tosto ma la legge del caos impone inesorabilmente l'occupazione degli spazi vuoti , e io di caos . . . me nč intendo .
. . . Non va bene , pessimo inizio, . . . ho incominciato dalla fine . . . . . . .
I Puntata
Tutto quello che cercherň di spiegare ruota su un'unica semplice formuletta .
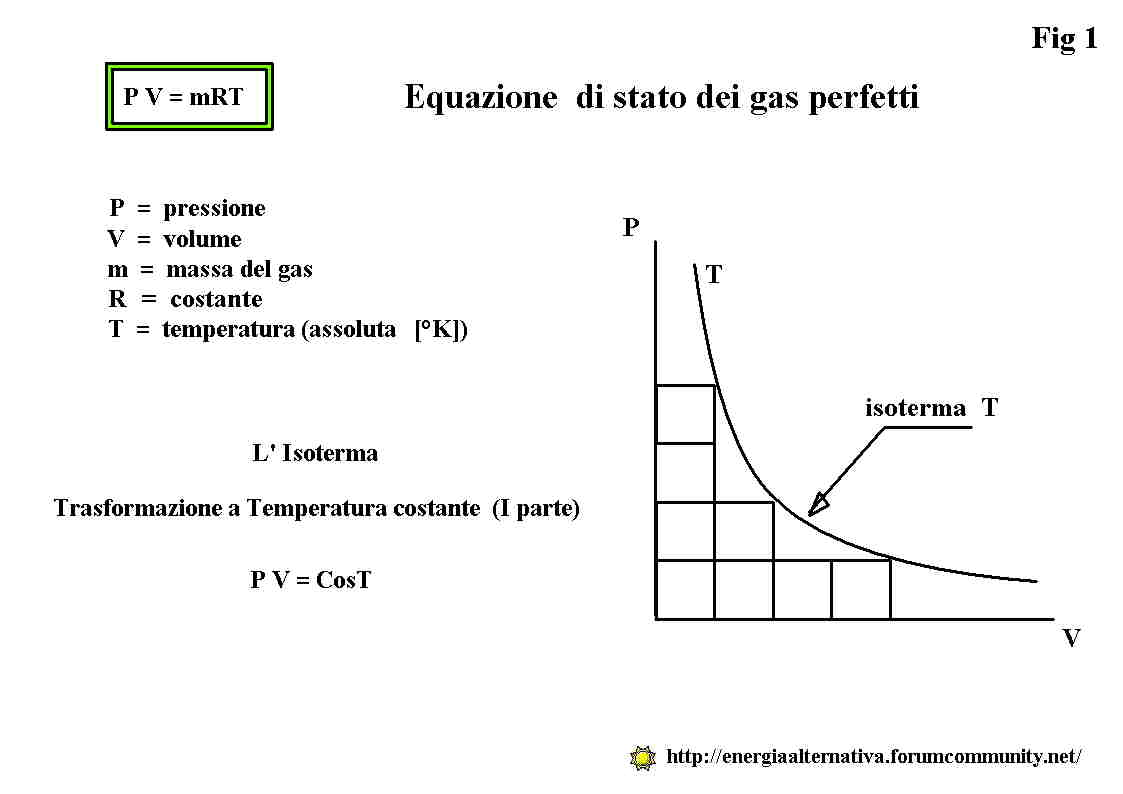
Si chiama : Equazione di stato dei gas perfetti :
P x V = m x R x T
http://it.wikipedia.org/wiki/Equazione_di_...ei_gas_perfetti
Niente paura , guardate solo le figure . . che adesso la formula . . . la smontiamo
Incominciamo col dire che m č la quantitŕ di gas, che supponiamo costante , R č una costante e T č la temperatura di quella quantitŕ di gas che per il momento supponiamo costante "pure lei".
Cosě non vale , esclama ad alta voce uno dal fondo ,  ma io faccio finta di non sentire . . . ma io faccio finta di non sentire . . .
se m , R e T sono costanti , il loro prodotto e anche costante (non cambia) ,e per esempio č uguale a CosT :
quindi se T e costante . . . . definiamo CosT = P x V .
Cosě č piu facile ? . . . andiamo avanti.
Quella formula, quel CosT . . . sembra l'area di un rettangolo con base V e altezza P . . . preciso preciso.
Quanti rettangoli possiamo disegnare con la stessa area ? . . . basta rimpicciolire la base ed aumentare l'altezza o viceversa in modo che il prodotto rimanga costante.
1 x 12
2 x 6
3 x 4
4 x 3
6 x 2
1 x 12
. . .
0,1 x 120
0,001 x 1200
. . . sono infiniti.
Bene se siete arrivati fin quě č probabile che arriveremo insieme alla fine . . . che non c'č.
Quel disegnino in alto a destra su wikipedia č un diagramma PV e quelle strane curve si chiamano "rami di iperbole equilatera " ma a noi questo non interessa. (per ora).
Prendete la prima curva , quella piů vicina all'origine degli assi.
Immaginate di disegnare un rettangolo con un vertice sull'origine e l'altro sulla curva.
Tutti i rettangoli che riuscirete a disegnare hanno la stessa area , se aumenta la base , diminuisce l'altezza e viceversa.
Quella curva, quel "ramo di iperbole" rappresenta l'area del rettangolo . . . costante , rappresenta CosT . ma come abbiamo definito CosT ? :
CosT = P x V = m x R x T ma siccome m e R sono costanti quel CosT rappresenta . . . la temperatura T
Adesso la figurina di Wikipedia č piů chiara , quella famiglia di curve che si allontanano dall'origine sono la rappresentazione grafica di temperature . . . crescenti.
Spiegheremo quel "crescenti" nelle prossime . . . puntate.
Un Saluto a tutti
Modificato da Libero51 - 21/3/2009, 15:56
|
| | |
Lupo cattivo
| Inviato il: 19/3/2009,15:52
|
Quello che bisbiglia dal fondo č un certo Johannes Diderik van der Waals , che continua a gridare delle cose in olandese che non capisco, ma credo ce l'abbia con te, Libero. 
Invece vedo due francesi, poi un altro francese accanto ad un inglese che approvano con grandi cenni del capo e dicono bravň, bravň... 
|
| | |
Libero51
| Inviato il: 21/3/2009,09:09
|
CITAZIONE (Lupo cattivo @ 19/3/2009, 15:52) . . . Johannes Diderik van der Waals , che continua a gridare delle cose in olandese che non capisco
Ciao a tutti , Diderik . . . silenzio.
II puntata : l'isobara
Nella prima puntata abbiamo visto il significato dell’isoterma che rappresenta per una data massa di gas m la relazione tra il suo volume V e la sua pressione P alla stessa temperatura T
Questa volta descriveremo il significato dell ‘isobara che rappresenta per la stessa massa di gas m la relazione tra il suo volume V e la sua temperatura T alla stessa pressione P .
Avevo promesso di usare la sola formula : PV = mRT
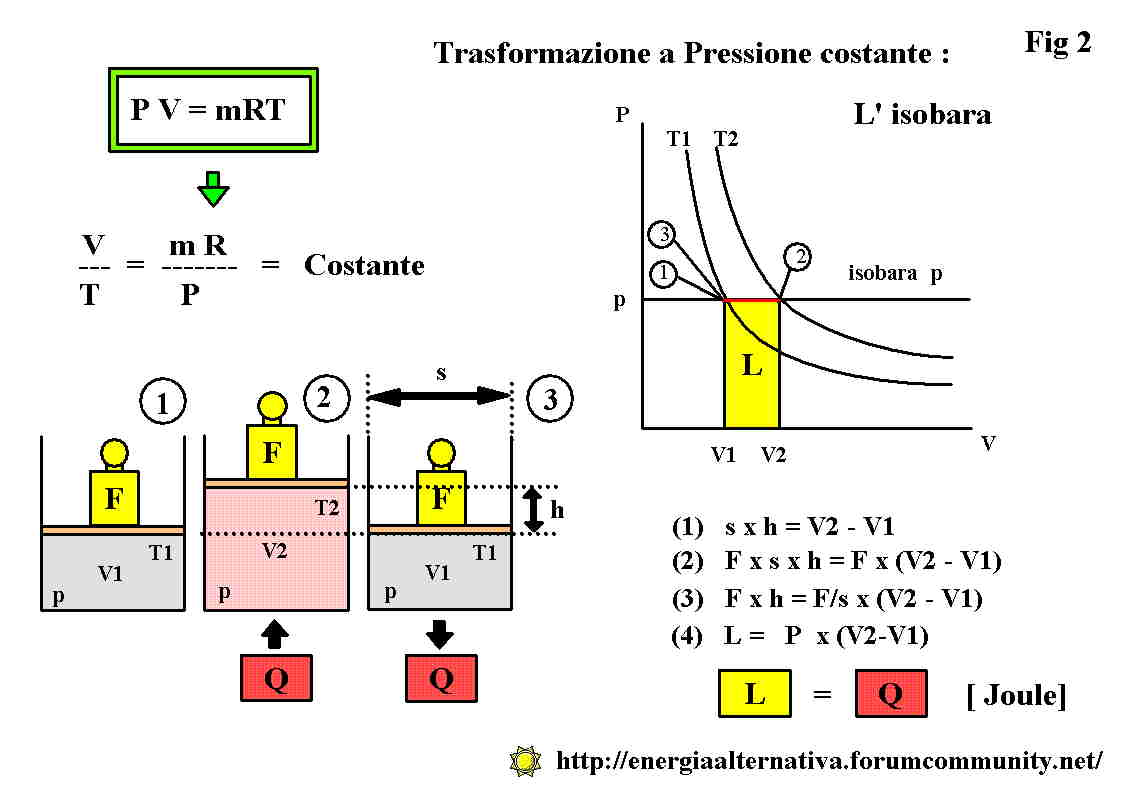
Nella figura in alto a sinistra si vede che in tale formula dividendo da entrambe le parti per PT si ottiene :
PV/PT = mrT /PT), semplificando : V/T = (mR)/P
In questo modo abbiamo portato a destra tutti I valori costanti e possiamo scrivere:
(*) V/T = costante
Fino a questo momento sembra piů una puntata di matematica che di termodinamica ma adesso viene il . . . bello.
Meno male . . . bisbiglia uno con i capelli verdi 
Nella “fase” 1 :
Prendiamo un cilindro di sezione s , con un leggerissimo pistone scorrevole e intrappoliamo l’aria al suo interno posando un peso F sul pistone . Abbiamo intrappolato la massa m di aria in un volume V1 alla temperatura T1. Il peso F agendo sulla superficie s del cilindro porta all’interno del cilindro la pressione dell’aria alla pressione P = F s. Guardando le fasi successive ci accorgiamo che il peso F non cambia e questo ci fa comprendere che in quello che vedremo la pressione non cambia mai.
Anche nel diagramma PV , a destra, la fase 1 indica un punto che corrisponde al volume V1 , che si trova sull’isoterma T1 e corrisponde a quella linea orizzontale che indica la pressione costante p.
Quella linea orizzontale č l’isobara p e la trasformazione che vedremo percorrerŕ il tratto rosso di tale isobara.
Nella fase 2
In questa fase scaldiamo , lentamente . . .
Perchč lentamente ? , chiede un giovane con i capelli dritti . . . i giovani si sŕ sono impazienti e amano la velocitŕ . chiede un giovane con i capelli dritti . . . i giovani si sŕ sono impazienti e amano la velocitŕ .
Bisogna che l'energia di movimento rimanga molto piccola , quasi nulla . L'energia di movimento o cinetica si calcola con . . . no non posso , ho promesso di usare una formula sola.
Non preoccupatevi avremo modo di tornare sull'argomento.
In questa fase scaldiamo , lentamente il cilindro fornendo un’energia termica corrispondente alla quantitŕ di calore Q. La temperatura sale lentamente al valore T2 . . .
Con il nostro marchingegno da un lato e con le nostra formula (*) dall’altro abbiamo imposto che la trasformazione avvenga a pressione costante.
A sinistra l’aria contenuta nel cilindro ,scaldandosi dalla temperatura T1 alla temperatura T2 ,si dilata ed aumentando il suo volume da V1 a V2 spinge verso l’alto il pistone ed il peso F del valore h.
Anche a destra, sul diagramma , il volume passa da V1 e V2 e la temperatura abbandona l’isoterma T1 e raggiunge l’isoterma T2.
Cercate di impadronirvi della relazione che esiste tra le fasi 1 e 2 del marchingegno a sinistra con la relazione tra le fasi 1 e 2 sul diagramma a destra.
Notate quanto č stato piů facile disegnare il diagramma rispetto al marchingegno.
Capisco che vi sembri piů difficile da capire ma se avrete la costanza di impadronirvene e proseguire avrete imparato un metodo potentissimo per valutare il funzionamento di una macchina termica . . . qualunque . . . a colpo d’occhio. (. . . scrivendo stň imparando anch’io)
Che cosa č successo ?
A sinistra : abbiamo fornito un’energia termica Q ed abbiamo sollevato un peso F ad un’altezza h. L’energia termica Q si č “magicamente” trasformata in . . . Lavoro meccanico.!!
oohhhhhhhhh . . . 
Il passaggio (1) indica che la variazione di volume V2-V1 č uguale al prodotto della superficie s del cilindro per l’altezza h , nei passaggi successivi si dimostra che il rettangolo giallo sul diagramma PV rappresenta il lavoro L prodotto dal sollevamento h del peso F.
Sul diagramma PV le superfici indicano energia !! . . , quelli col cappelletto sono tutti contenti . . 
Il rettangolo giallo č la rappresentazione meccanica dell’energia L fornita al marchingegno dall’energia termica Q.
Nella fase 3 :
L’energia termica Q viene sottratta dal marchingegno , raffreddandolo, in modo che la temperatura ritorni a T1 ed il volume a V1.
(continua . . .) 
Un saluto a tutti
Modificato da Libero51 - 21/3/2009, 15:51
|
| | |
NonSoloBolleDiAcqua
| Inviato il: 21/3/2009,09:43
|
CITAZIONE (Libero51 @ 21/3/2009, 09:09) CITAZIONE (Lupo cattivo @ 19/3/2009, 15:52) . . . Johannes Diderik van der Waals , che continua a gridare delle cose in olandese che non capisco Ciao a tutti , Diderik . . . silenzio.

---------------
Chi sa raccontare bene le bugie ha la veritŕ in pugno (by PinoTux).
Un risultato se non č ripetibile non esiste (by qqcreafis).
|
| | |
Libero51
| Inviato il: 24/3/2009,08:32
|
Riassunto delle precedenti puntate:
I puntata : L'isoterma nel diagramma PV indica una temperatura costante ed un prodotto P x V = costante.
II puntata: L'isobara nel diagramma PV indica una pressione costante e l'area del diagramma indica energia.
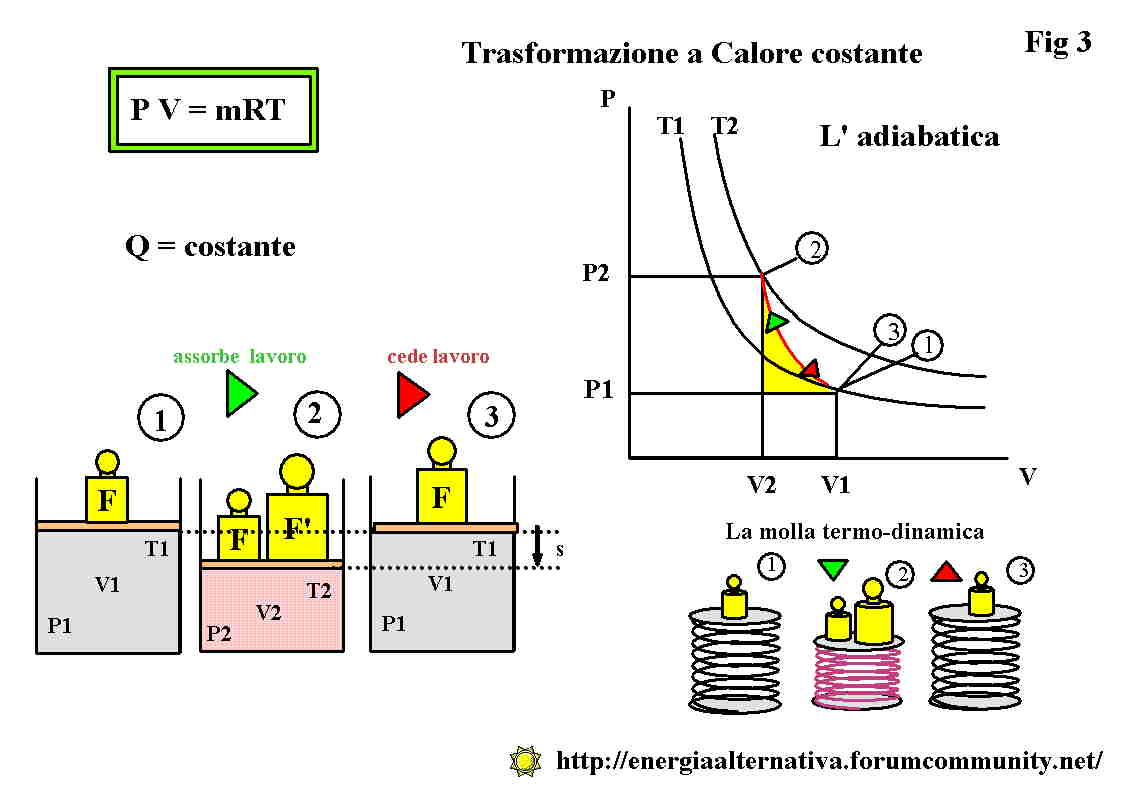
III puntata : l'adiabatica
Una trasformazione adiabatica avviene senza che il nostro marchingegno perda o ossorba calore dall'esterno. Una tale trasformazione č possibile con un isolamento infinito del marchingegno o con una velocitŕ infinita (tempo = 0). In entrambi i casi il calore non viene trasmesso con l'esterno.
Un'esempio di trasformazione "quasi" adiabatica č la fase di scoppio di un motore . . . a scoppio.
Tale evento rapidissimo ed il calore ,"quasi" non ha il tempo di propagarsi.
In questa puntata , non "useremo" la formula di stato . . .
Meno male . . . bisbiglia il solito con i capelli verdi 
Stiamo imparando , me compreso, come funziona un motore a molla . . . a molla ?  . . . acc...... ho sbagliato discussione. . . . acc...... ho sbagliato discussione.
. . .una molla particolare . . . una molla termodinamica.
I giovani forse non hanno giocato con le macchinine a molla, carichi la chiavetta e la macchinina parte e quando la carica finisce la macchinina . . . si ferma.
La molla termodinamica funziona come una molla normale ma se la scaldi si irrobustisce e se la raffreddi si indebolisce. Tutto quě .
Nella fase 1-2 :
aggiungendo un peso F' sul pistone e sulla molla entrambi si accorciano di un tratto s e quindi in entrambi i casi , per ottenere tale deformazione č necessario fornire un lavoro L = F' x s .
L'aria contenuta nel cilindro si comprime , la pressione sale , e si scalda . . . quel lavoro fornito si trasforma in calore .
Il calore č intrappolato nella trasformazione adiabatica (senza scambio di calore) e la temperatura . . . aumenta dal valore T1 al valore T2 , piů elevato . osservate come sul diagramma la freccia verde in salita indica un lavoro assorbito dalla trasformazione . L'isoterma T1 viene abbandonata viene raggiunta progressivamente l'isoterma T2.
La molla termodinamica si č accorciata e si č anche irrobustita dal crescere della temperatura.
Notate che il peso F' č piů grande di F , su questa cosa ci torneremo . . .
L'area gialla nel diagramma indica il lavoro assorbito dalla trasformazione e trasformato in calore.
Nella fase 2-1:
Il peso F' viene tolto ed il cilindro restituisce il lavoro accumulato in calore . La temperatura diminuisce ritornando a T1 e sul diagramma la freccina rossa in discesa indica appunto che il lavoro viene restituito. Anche la nostra molla termodinamica restituisce l'energia accumulata e raffreddandosi ritorna alla "debolezza" iniziale.
Qualcuno si chiederŕ perchč ho introdotto questo concetto di molla termodinamica.
E' un ennesimo tentativo di spiegare un fenomeno sconosciuto paragonandolo ad uno ben noto.
Senza considerare attriti la molla della macchinina restituisce l'energia che abbiamo usato per caricarla.
Se la molla della macchinina fosse termodinamica potremmo consumare poca energia per caricare la molla "fredda" e debole, scaldarla e rafforzarla, usare la scarica della molla "calda" e robusta e risparmiare un pň di scarica .
Per farne cosa ?
Alla fine della scarica , dovremmo raffreddarla ed indebolirla ed usare l'energia che abbiamo messo da parte per ricaricarla.
In questo modo non dovremmo piů ricaricare la molla "manualmente", una volta avviata la macchinina continuerebbe a girare solo con il ripetuto riscaldamento e raffreddamento della molla termodinamica.

Avremmo bisogno solo di una sorgente di "calore" per scaldarla ed una sorgente di "freddo" per raffreddarla.
Ma questa č la simulazione a molla di una macchina termodinamica.
oohhhhhhhhh . . . 
(continua)
Un saluto a tutti
Modificato da Libero51 - 26/3/2009, 00:31
|
| | | | | | |
Libero51
| Inviato il: 28/3/2009,07:34
|
Riassunto delle precedenti puntate:
I puntata : L'isoterma(I parte) nel diagramma PV indica una temperatura costante ed un prodotto P x V = costante.
II puntata: L'isobara nel diagramma PV indica una pressione costante e l'area del diagramma indica energia.
III puntata :L'adiabatica nel diagramma PV indica una trasformazione senza scambio di calore
IV puntata :L'isoterma (II parte)
V puntata : l'isocora
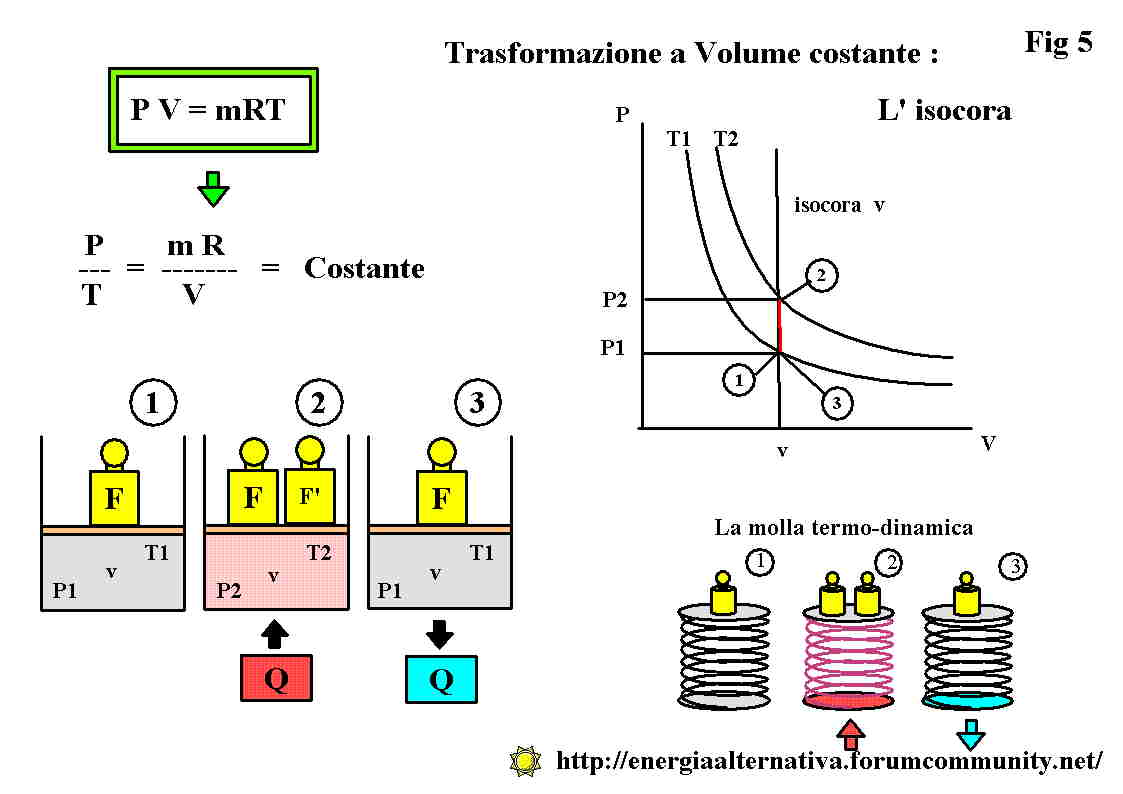
In questa puntata descriveremo il significato dell ‘isocora che rappresenta per la stessa massa di gas m la relazione tra la sua pressione P e la sua temperatura T senza cambiare il Volume .
Trasformando la solita unica formula : PV = mRT
dividendo da entrambe le parti per VT si ottiene :
PV/VT = mrT /VT), semplificando : P/T = (mR)/V
In questo modo abbiamo portato a destra tutti I valori costanti e possiamo scrivere:
P/T = costante
Ho capito adesso . . . , se due cose sono uguali e le modifichi entrambe nello stesso modo riottieni due cose uguali ! . . . 
Nella trasformazione 1-2 forniamo progressivamente al nostro cilindro una quantitŕ di calore Q.
Appena incominciamo la pressione tende a salire ed il pistone a sollevarsi. Per impedire che il pistone si muova ,mano a mano che forniamo calore aggiungiamo ulteriore peso sul pistone. Alla fine avremo aggiunto complessivamente un peso F' .
L'aria od il gas contenuto nel cilindro non puň espandersi e l'energia Q che abbiamo fornito provoca un'aumento di pressione da P1 a P2 ed un aumento di temperatura da T1 a T2 .
Durante tutto il tempo della trasformazione :
P1/T1 = P1' / T1'= P1''/T1''= . . . . . . . P2/T2= costante
La stessa cosa succede alla nostra molla termodinamica che non ha potuto espandersi e si č irrobustita con l'aumento della temperatura ; per non farla espandere , anche con lei, abbiamo dovuto , nello stesso modo, aggiungere un ulteriore peso F'.
Nella trasformazione 2-3 sottraendo calore e togliendo progressivamente peso dal cilindro e dalla molla termodinamica si ritorna alle condizioni inizali.
E' interessante notare che in questa trasformazione non viene compiuto nessun lavoro meccanico proprio perchč non c'č spostamento.
In questa puntata abbiamo visto l'ultima trasformazione collegata alla formula di stato dei gas perfetti.
Che bello abbiamo finito . . . 
No no , non abbiamo finito . . . adesso possiamo incominciare.
come . . . possiamo incominciare ? 
Sarŕ una mia impressione ma ha i capelli piů dritti del solito.
Adesso conosciamo le singole trasformazioni elementari per comprendere il funzionamento completo di una macchina termica.
Quando avrete dei dubbi ritornate su queste puntate e anche solo guardando le figure č probabile che i dubbi , piano piano si risolvino.
Nella prossima puntata vedremo il ciclo completo teorico del motore stirling e poi , se vorrete, andremo avanti . . .
questa volta sono stati tutti zitti . . . .
(continua)
Un saluto a tutti
|
| | |
Libero51
| Inviato il: 5/4/2009,08:16
|
CITAZIONE (Libero51 @ 28/3/2009, 08:34) Riassunto delle precedenti puntate:
I puntata : L'isoterma(I parte) nel diagramma PV indica una temperatura costante ed un prodotto P x V = costante.
II puntata: L'isobara nel diagramma PV indica una pressione costante e l'area del diagramma indica energia.
III puntata :L'adiabatica nel diagramma PV indica una trasformazione senza scambio di calore
IV puntata :L'isoterma (II parte)
V puntata :L'isocora
VI puntata : Il Ciclo Stirling teorico
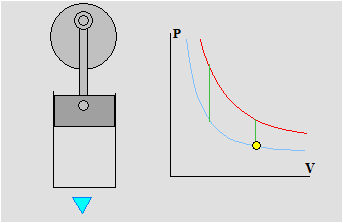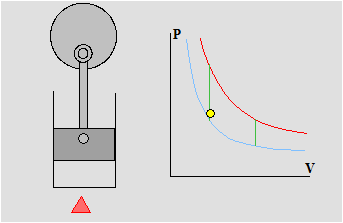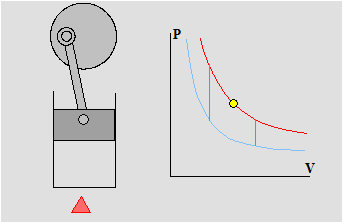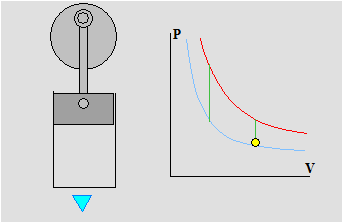
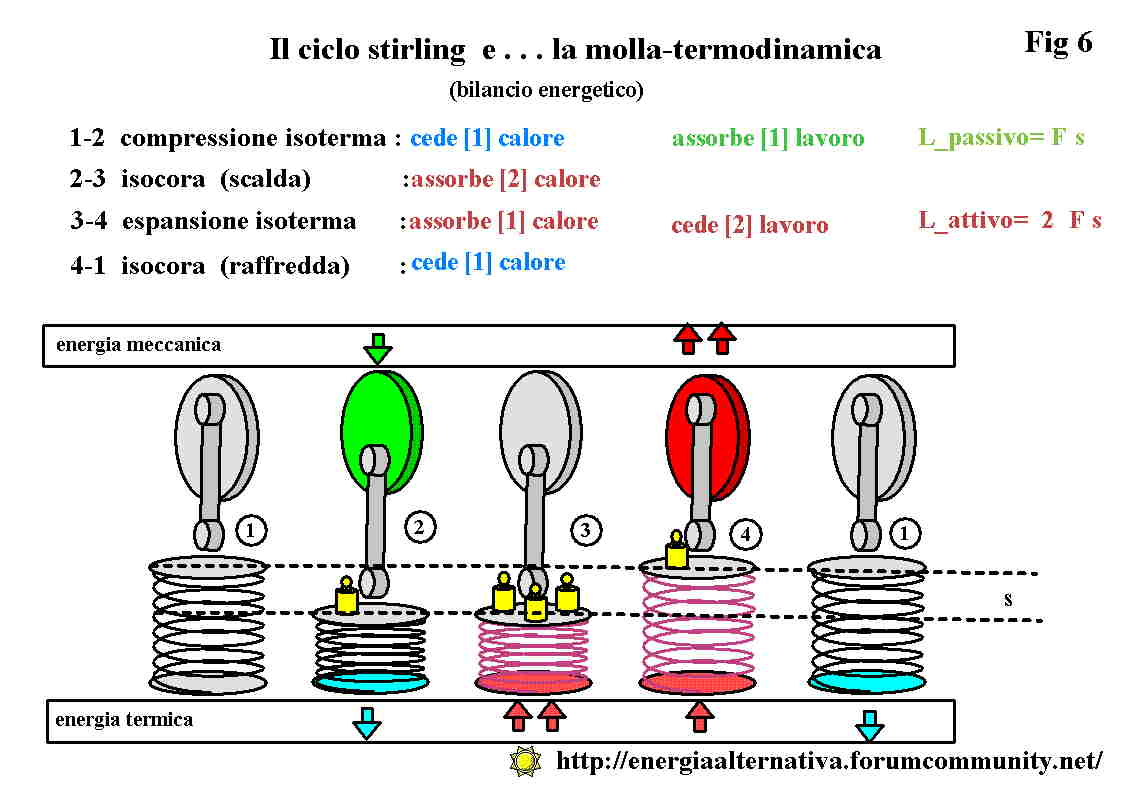
Dopo aver visto le trasformazioni principali sul diagramma PV possiamo ora analizzare il ciclo completo Stirling teorico composto solo da isoterme ed isocore .
Come potete osservare nell'animazione le trasformazioni isoterme (rossa e blů ) avvengono con variazione di volume ed infatti durante tali trasformazioni il pistone si muove. Durante le isocore ( verdi ) il pistone si ferma e aspetta che la temperatura cambi tra le due isoterme. Abbiamo spiegato all'inizio che l'area racchiusa nel ciclo č proporzionale all'energia sviluppata ed in queste condizioni , non realisticamente realizzabili l'area č la massima possibile. La rapiditŕ con la quale avviene il cambio della temperatura č quindi un elemento fondamentale per costruire motori efficienti. Il motore della nostra macchina , sia durante la fase di scoppio (riscaldamento rapido) che durante la fase di scarico (raffreddamento rapido) realizza ottimamente questa condizione. . . ma questa č un'altra storia.
Questo piccolo e veloce racconto della termodinamica letta sul diagramma PV ha lo scopo di introdurre le soluzioni che i vari tipi di motore Stirling adottano per poter funzionare.
Sul Web si trovano facilmente simulazioni e realizzazioni di tutti i tipi.
. . . continua . . .
Un saluto a tutti-
|
| | |
qqcreafis
| Inviato il: 2/2/2010,19:48
|
completiamo..........................................................................
Gas perfetto insieme di "punti" dotati di massa che sono in equilibrio termico con le pareti.
Modello piů evoluto i punti possono "essere" anche poliatomici questo implica che oltre a traslare possono anche vibrare ruotare ecc ecc.
Nel modello si trascura il fatto che le molecole si possano urtare e che le molecole possano esercitare una forza le une sulle altre.
Significa che un gas perfetto non cambia mai di stato. Se viene tolta l'energia cinetica di traslazione il gas collassa ad uno stato di pressione e volume nullo
Si studia il gas perfetto perchč tutti i gas si comportano come il gas perfetto se opportunamente rarefatto e lontano da temperature di passaggio di stato.
L'energia interna di un gas perfetto č cinetica di traslazione e di rotazione ed altro .
L'energia interna dipende solo e unicamente dalla temperatura
La temperatura č una misura della sola energia cinetica di traslazione
La variazione di energia interna si puň calcolare tramite un calore specifico
---------------
ODE AD UNO STUDENTE MERITEVOLE (Sermone)
Allora Xyz č stato bravo! noi dobbiamo riconoscere che č stato molto bravo, bisogna dirlo !
In un mondo dove tutto SEMBRA uguale a tutto.
In un mondo dove chi abbruttisce la dignitŕ dell’intelligenza umana si arroga meriti.
In un mondo in cui si dice che i giovani non hanno speranza perché “tanto non troveranno lavoro” perché tanto non “non avranno la pensione”.
Xyz č stato bravo! ha capito tutto, ha fatto un compito perfetto.
Xyz ci da una SPERANZA.
Xyz non ha seguito le falsitŕ che ci circondano.
Xyz si č impegnato ed č riuscito nel suo intento.
|
| | |
qqcreafis
| Inviato il: 2/2/2010,20:15
|
un calore specifico a volume costante detto Cv
Il calore specifico a volume costante č (numericamente) uguale alla quantitŕ di energia necessaria per far variare di 1K la temperatura di una mole di gas, mantenedo il volume costante durante il processo
Per un gas monoatomico Cv=3/2R biatomico 5/2R dove R= 8,31j/(k*mol)
Un sistema termodinamico puň scambiare calore e lavoro
---------------
ODE AD UNO STUDENTE MERITEVOLE (Sermone)
Allora Xyz č stato bravo! noi dobbiamo riconoscere che č stato molto bravo, bisogna dirlo !
In un mondo dove tutto SEMBRA uguale a tutto.
In un mondo dove chi abbruttisce la dignitŕ dell’intelligenza umana si arroga meriti.
In un mondo in cui si dice che i giovani non hanno speranza perché “tanto non troveranno lavoro” perché tanto non “non avranno la pensione”.
Xyz č stato bravo! ha capito tutto, ha fatto un compito perfetto.
Xyz ci da una SPERANZA.
Xyz non ha seguito le falsitŕ che ci circondano.
Xyz si č impegnato ed č riuscito nel suo intento.
|
| | |
qqcreafis
| Inviato il: 2/2/2010,21:16
|
Il calore che entra č conteggiato + positivo il calore che esce č conteggiato - negativo
Il Lavoro che entra č conteggiato - negativo il lavoro che esce + positivo
Per ricordarsi il segno basta pensare ad un motore l'energia che entra come calore ed il lavoro prodoto positivo, il calore perso ed il lavoro assorbito (es compressione) negativo.
Se un sistema assorbe o cede energia la variazione di energia interna č = all'energia entrata - energia uscita , in altri simboli
Delta U = Q-L
1° principio della temodinamica conseguenza del fatto che l'energia non scompare o non si crea dal nulla. (N.b. il segno meno č conseguenza del segno scambiato per il lavoro)
---------------
ODE AD UNO STUDENTE MERITEVOLE (Sermone)
Allora Xyz č stato bravo! noi dobbiamo riconoscere che č stato molto bravo, bisogna dirlo !
In un mondo dove tutto SEMBRA uguale a tutto.
In un mondo dove chi abbruttisce la dignitŕ dell’intelligenza umana si arroga meriti.
In un mondo in cui si dice che i giovani non hanno speranza perché “tanto non troveranno lavoro” perché tanto non “non avranno la pensione”.
Xyz č stato bravo! ha capito tutto, ha fatto un compito perfetto.
Xyz ci da una SPERANZA.
Xyz non ha seguito le falsitŕ che ci circondano.
Xyz si č impegnato ed č riuscito nel suo intento.
|
| | |
qqcreafis
| Inviato il: 2/2/2010,21:51
|
Lavoro scambiato in seguito ad una picola variazione di volume in una trasformazione qualunque
dL=P*dV (si puň leggere lavoro = pressione *variazione di volume)
calcolo lavoro e calore scambiato nelle varie trasformazioni e variazione energia interna
Isocora
def V=cost
L=0J (dato che non c'č variazione di volume e quindi spostamento (la forza c'č perchč c'č la pressione))
Q=n*Cv*(Tfinale-Tiniziale) ( esattamente uguale alla variazione di energia interna)
S= integrale da Ti aTf dq/T=n*Cv*ln(Tf/Ti)=n*Cv*ln(Pf/Pi)
Isobara
def P=cost
L=P*(Vf-Vi) (lavoro scambiato = pressione *variazione di Volume)
Q = n*Cv*(Tf-Ti)+P*(Vf-Vi)=n*Cv(Tf-Ti)+ n*R*(Tf-Ti)=n*(Cv+R)*(Tf-Ti)=n*Cp*(Tf-Ti)
(il calore che entra non solo va a riscaldare ma esce anche come lavoro )
Cp colore specifico a pressione costante, numericamente uguale all'energia necessaria per far aumentare di 1K una mole di gas a pressione costante
Delta S= integrale da Ti aTf dq/T=n*Cp*ln(Tf/Ti)=n*Cp*ln(Vf/Vi)
Isoterma
def T=cost
L=Q ( il Lavoro scambiato č uguale al Calore scambiato in quanto non essendoci variazione di Temperatura non c'č variazione energia interna, se entrano 10j di calore (+) devono uscire 10j (+) di Lavoro e viceversa)
---------------
ODE AD UNO STUDENTE MERITEVOLE (Sermone)
Allora Xyz č stato bravo! noi dobbiamo riconoscere che č stato molto bravo, bisogna dirlo !
In un mondo dove tutto SEMBRA uguale a tutto.
In un mondo dove chi abbruttisce la dignitŕ dell’intelligenza umana si arroga meriti.
In un mondo in cui si dice che i giovani non hanno speranza perché “tanto non troveranno lavoro” perché tanto non “non avranno la pensione”.
Xyz č stato bravo! ha capito tutto, ha fatto un compito perfetto.
Xyz ci da una SPERANZA.
Xyz non ha seguito le falsitŕ che ci circondano.
Xyz si č impegnato ed č riuscito nel suo intento.
|
| | |
qqcreafis
| Inviato il: 2/2/2010,23:02
|
L=integrale Vi a Vf P*dV=n*R*T* integrale da Vi a Vf dV/V=n*R*T*ln(Vf/Vi)=n*R*T*ln(Pi/Pf)
S=Q/T=n*R*ln(Pi/Pf)=n*R*ln(Vf/Vi)
Adiabatica
def Q=0J ( non c'č scambio di calore, perň c'č scambio di Lavoro a spese o ad incremento energia interna ( Delta U = -L) se c'č un'espansione l'energia interna (temperatura) crolla, se c'č una compressione l'energia interna (temperatura)aumenta, ad es. In un diesel nella fase di compressione l'aria passa da T ambiente a 700 °C!!)
L= -n*Cv*(Tf-Ti)
il calcolo del lavoro deriva dal calcolo dell'energia interna
e dato che mi voglio proprio male espansione libera
Espansione di un gas in assenza di alcunchč che tolga energia ( da non confondersi con l'adiabatica)
Q=0
L=0
Delta U =0 (la temperatura non cambia!!!)
Delta S come nell'isoterma!
 scorciatoie e definizioni importanti scorciatoie e definizioni importanti 
Variabile di stato
Grandezza fisica che dipende solo dallo stato attuale del sistema come la Temperatura, l'energia interna , pressione
Lo stato nel grafico PV č un punto! (punto nell'area)
Controesempio il Lavoro dipende da quello che successo
Perchč tutto sto casino????????????
Perchč voglio calcolare il rendimento dello Stirling e l'ho presa un pň larga...
alla prossima
---------------
ODE AD UNO STUDENTE MERITEVOLE (Sermone)
Allora Xyz č stato bravo! noi dobbiamo riconoscere che č stato molto bravo, bisogna dirlo !
In un mondo dove tutto SEMBRA uguale a tutto.
In un mondo dove chi abbruttisce la dignitŕ dell’intelligenza umana si arroga meriti.
In un mondo in cui si dice che i giovani non hanno speranza perché “tanto non troveranno lavoro” perché tanto non “non avranno la pensione”.
Xyz č stato bravo! ha capito tutto, ha fatto un compito perfetto.
Xyz ci da una SPERANZA.
Xyz non ha seguito le falsitŕ che ci circondano.
Xyz si č impegnato ed č riuscito nel suo intento.
|
| | |
qqcreafis
| Inviato il: 3/2/2010,12:47
|
I cicli
Una trasformazione ciclica č una trasformazione che ritorna alloa stato di partenza
---------------
ODE AD UNO STUDENTE MERITEVOLE (Sermone)
Allora Xyz č stato bravo! noi dobbiamo riconoscere che č stato molto bravo, bisogna dirlo !
In un mondo dove tutto SEMBRA uguale a tutto.
In un mondo dove chi abbruttisce la dignitŕ dell’intelligenza umana si arroga meriti.
In un mondo in cui si dice che i giovani non hanno speranza perché “tanto non troveranno lavoro” perché tanto non “non avranno la pensione”.
Xyz č stato bravo! ha capito tutto, ha fatto un compito perfetto.
Xyz ci da una SPERANZA.
Xyz non ha seguito le falsitŕ che ci circondano.
Xyz si č impegnato ed č riuscito nel suo intento.
|
| | |
qqcreafis
| Inviato il: 3/2/2010,13:55
|
Un motore segue sempre una trasformazione ciclica ad es. dopo due giri dell'albero motore un 4 tempi si ritrova al punto di partenza
Una trasformazione ciclica nel diagramma P-V č rappresentata da una curva chiusa ( E' ovvio dato che si ritorna allo stato di partenza)
Proprietŕ dei cicli
Dato che si ritorna sempre nello stato di partenza la variazione totale ( calcolata su tutto il ciclo) di una qualunque variabile di stato č sempre zero
Cosa ci dice l'energia interna?????????????????????????
Variazione di energia interna su tutto il ciclo = 0
(dal punto di vista fisico se rimanesse il un pň di energia ad ogni ciclo il motore fonderebbe, oppure rangiungerebbe lo zero assoluto)
Deduzione importantissima!
dal primo principio della dinamica Delta U = Q-L
su tutto il ciclo allora
0=Q-L ovvero Q=L
significa che su tutto un ciclo
Calore scambiato = Lavoro scambiato
deduzione che ci aiuterŕ nel calcoli del rendimento di un motore (che contenga trasformazioni note)
cose analoghe si possono fare con l'entropia S
Rendimento di un motore
Rendimento = (Lavoro prodotto)/ (energia utilizzata)
č in altre porole il rapporto tra l'energia prodotta come lavoro e l'energia utilizzata.
Il rendimento puň varaiare tra 0 ed 1 . Se il rendimento č 0 significa che il motore non prodoce lavoro se 1 significa che tutta l'energia utilizzata č tradotta il Lavorro utile
Il 2° principio della termodinamica vieta che il rendimento di un motore sia = 1
Il rendimento di un motore č sempre <1
---------------
ODE AD UNO STUDENTE MERITEVOLE (Sermone)
Allora Xyz č stato bravo! noi dobbiamo riconoscere che č stato molto bravo, bisogna dirlo !
In un mondo dove tutto SEMBRA uguale a tutto.
In un mondo dove chi abbruttisce la dignitŕ dell’intelligenza umana si arroga meriti.
In un mondo in cui si dice che i giovani non hanno speranza perché “tanto non troveranno lavoro” perché tanto non “non avranno la pensione”.
Xyz č stato bravo! ha capito tutto, ha fatto un compito perfetto.
Xyz ci da una SPERANZA.
Xyz non ha seguito le falsitŕ che ci circondano.
Xyz si č impegnato ed č riuscito nel suo intento.
|
|
| | |
|
Versione Mobile!
 

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|





